
早上起床量血壓、戴上隱形眼鏡出門、坐在診療椅上接受植牙手術,這些看似平凡的日常片段,都與醫療器材密不可分。唯有安全、可靠的醫療器材,才能在診斷、治療與日常健康管理中穩定發揮,協助醫療行為順利進行。醫材的可靠不只來自器材本身的功能,更來自背後一整套嚴謹的安全把關與管理機制。
上市前:嚴格准入審查與可追溯性
每一件醫療器材在進入診間、手術室與家庭之前,都必須先經過一道道嚴格的審查與把關,確保產品來源清楚、合法合規。
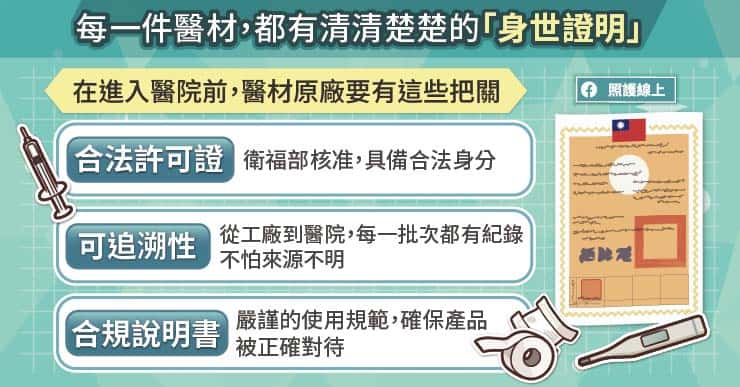
首先,每一件醫療器材都必須取得衛福部核發的「醫療器材許可證」。這張許可證代表該醫材的安全性、有效性及品質控管均符合國家標準。不僅如此,為了進一步降低風險,合法原廠醫材須具備嚴謹的可追蹤紀錄,從原料採購、生產製造、品質檢驗到物流運送,每一個環節都有清楚的紀錄與編號。這種具備「履歷」的管理方式,能在發生異常的第一時間迅速追溯源頭,也可嚴絕來源不明的零件混入。
此外,醫療器材也附有專業且詳盡的產品說明與使用指引,可視為安全使用的重要依據。內容會清楚標示適用情況、操作方式、禁忌事項及可能風險。當專業團隊能清楚掌握「該怎麼用、不該怎麼用、什麼時候可以用、什麼時候不能用」時,便能有效避免因使用不當產生的醫療風險。
上市後:專業技術支援與持續監測
醫療器材進入市場後,相關的安全監測仍會持續進行。為了將人為操作疏失降至最低,原廠會針對醫事人員提供標準化的訓練課程,內容涵蓋設備組裝、參數調整與維護規範。在臨床端遇到技術疑慮時,原廠專業團隊亦會即時介入,提供明確的操作指引,確保醫療行為在安全狀態下完成。
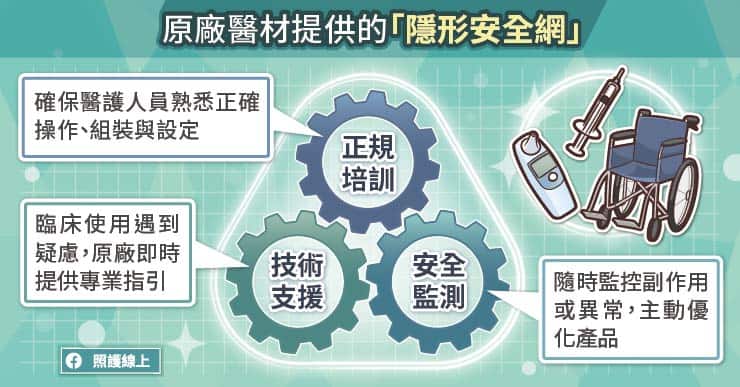
更重要的是,原廠通常也會在醫療器材上市後,持續建立安全監測與回饋機制,透過醫護人員在臨床第一線的使用經驗與回報,掌握器材在實際應用中是否出現副作用、異常狀況,或其他需要注意的風險。這些從教育訓練、技術支援,到上市後監測與異常通報的機制,並不是特定類型業者才有,而是任何重視品質管理與使用者安全的醫材廠商都應具備的基本責任。

完善安全網:區分不同醫材的通報機制
最後提醒大家,守護醫材安全需要醫、病與廠商三方的共同參與。所有醫療器材都有對應的通報管道,但依據產品屬性與使用情境,通報責任與方式有所區別:
針對「一般(院內)醫療器材」,若在臨床使用上涉及嚴重不良事件,根據《醫療器材嚴重不良事件通報辦法》規定,醫療機構與廠商具備法律義務,必須於法定期限內主動向食藥署(TFDA)進行通報。
至於民眾在居家使用的血壓計、血糖機等「家用醫療器材」,若發現產品異常或疑似不良反應,則仰賴使用者主動通報。民眾可利用食藥署「全國藥物不良反應通報中心」系統或撥打諮詢專線,讓管理單位能及早阻斷風險,維護全民健康。
重點筆記
● 合規准入審查:醫材須取得許可證,並具備可追溯生產履歷與專業操作說明書。
● 上市後專業支援:原廠提供醫護培訓與即時技術諮詢,並建立持續監測機制以優化安全性。
● 通報法規責任:醫事機構及廠商發現嚴重不良事件時,須依法定期限向主管機關通報。
● 民眾參與守護:居家醫材若有異常,民眾可主動透過網路通報系統或專線(02-2396-0100)反映。


