
「醫師,這是我一年多來第一次解出成形的糞便耶!」30歲的廖先生很開心地說。他因為反覆拉肚子,已經跑過很多醫院,後來又因為腹痛、發燒,接受過盲腸切除手術,但在術後,症狀仍舊反反覆覆,體重快速減輕,甚至在會陰部出現很深的潰瘍,持續流出渾濁的膿汁。
經過一系列的檢查,才終於確診克隆氏症,並開始使用免疫調節藥物治療。但是,輔仁大學附設醫院胃腸肝膽內科郭震亞醫師回憶,由於傳統藥物的治療成效不佳,所以再幫病患申請健保給付的腸道專一型生物製劑,病況終於漸漸穩定。目前患者各項發炎指數都在正常範圍,會陰部瘻管重新癒合,生活品質大幅改善。
腸道持續發炎,可不只有拉肚子
郭震亞醫師指出,發炎性腸道疾病屬於一種自體免疫疾病,腸道在受到外來刺激(例如細菌、食物、藥物、環境刺激等)之後,造成免疫功能錯亂,患者自己的免疫細胞開始攻擊正常的腸道黏膜,導致腸子發炎、潰爛,而出現慢性腹痛、腹瀉、血便等症狀。
發炎性腸道疾病可以分為兩種型態,包括潰瘍性大腸炎和克隆氏症。「潰瘍性大腸炎」的發炎只侷限在直腸和大腸,除了拉肚子之外,還會有間歇性的急便感、血便和慢性腹痛,長期下來會導致貧血、精神不濟的狀況,如果嚴重發炎會導致發燒,甚至腸道壞死而需要手術切除大腸。
「在臺灣,潰瘍性大腸炎好發於30至50歲的青壯人口,以男性較多,」郭震亞醫師說,「如果沒有好好治療,將會對家庭和社會造成很大的損失,日本前首相安倍晉三就是因為潰瘍性大腸炎而辭職下台。」
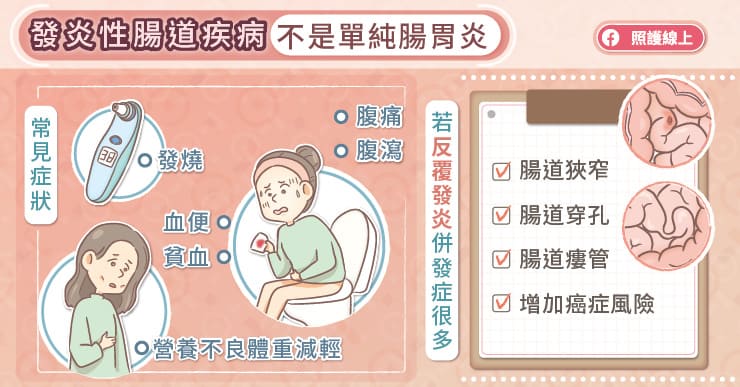
「克隆氏症」可以在所有消化器官造成發炎,包括口腔、食道、胃、小腸、大腸等,郭震亞醫師說,克隆氏症除了造成病患慢性腹痛、拉肚子之外,更常出現精神不濟、體重減輕和發燒等全身性症狀。由於克隆氏症的發炎較潰瘍性大腸炎更深,容易造成腸道穿孔、瘻管或狹窄等併發症。
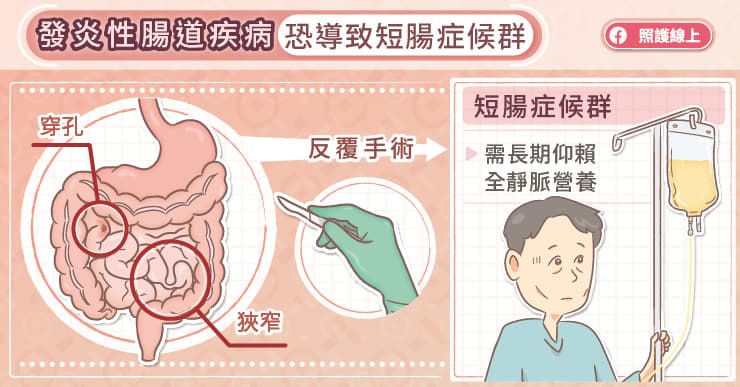
在台灣,克隆氏症好發在20至30歲的年輕人,也是以男性居多。克隆氏症如果沒有積極治療控制發炎,最終會有六成患者需要接受手術切除腸道,對身心造成莫大傷害。若因為併發症而反覆切除腸道,可能導致「短腸症候群」。
「短腸症候群」是指小腸因為大範圍的慢性發炎或手術切除而喪失消化、吸收功能,導致患者營養不良而需要終身接受靜脈或腸道營養補充。也因此,郭震亞醫師提醒,克隆氏症病友更需要積極治療控制腸道發炎,降低需要切除腸道的風險,以避免短腸症候群的發生。
除了腸道發炎之外,大約一到四成的發炎性腸道疾病患者會出現腸道外器官的發炎,例如眼睛發生葡萄膜炎或鞏膜炎、口腔慢性潰瘍、皮膚出現不正常的紅斑或潰爛,手指、脊椎或髖關節因慢性發炎而疼痛,另外,這種疾病也可能造成肝臟、膽道發炎,而在抽血時發現肝膽指數異常。
穩定控制,治療達標
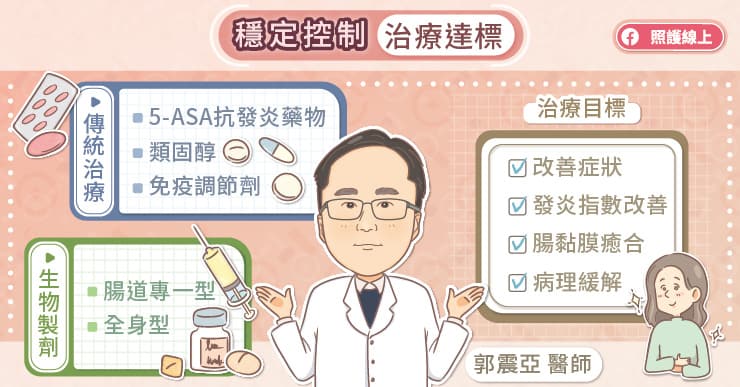
無論克隆氏症或潰瘍性大腸炎,較嚴重的急性期治療會先使用全身性類固醇來快速減輕發炎,若類固醇的治療成效不佳,則會考慮使用生物製劑或免疫抑制藥物作為第二線治療。
若是屬於輕度至中度的潰瘍性大腸炎,可使用5-ASA抗發炎藥物做為第一線藥物,如果療效不佳會考慮使用類固醇治療。郭震亞醫師解釋,克隆氏症對5-ASA抗發炎藥物的反應較差,即使是輕度發炎,在急性期仍然會以類固醇作為第一線治療。
由於長期使用全身性類固醇會造成新陳代謝方面的副作用,並增加感染的風險,因此不適合作為維持緩解的長期用藥,必須逐步替換為副作用較少的5-ASA抗發炎藥物或免疫調節劑來控制發炎。倘若傳統治療成效不佳,則會進一步使用生物製劑來長期控制發炎。
生物製劑是種單株抗體,可以阻斷特定發炎路徑以達到抑制發炎的效果,相較於類固醇,生物製劑的專一性、安全性較高,也會比傳統免疫調節劑的療效更穩定,但由於藥價昂貴,因此目前在臺灣健保給付中屬於第二線治療。
生物製劑藥物主要可分為兩種機轉,全身型生物製劑可抑制發炎介質作用,腸道專一型生物製劑可抑制淋巴球遷徙至腸道組織而達到抗發炎作用。郭震亞醫師指出,腸道專一型生物製劑主要是針對腸道的發炎反應做抑制,較不影響其他器官的免疫反應,長期使用時感染風險較低,是目前生物製劑中較安全的選擇。
生物製劑的療效和發炎性腸道疾病的嚴重度、患者本身的狀況有關,郭震亞醫師分析,平均而言,使用生物製劑治療中重度潰瘍性大腸炎,約有6成患者可維持腸道黏膜癒合;治療克隆氏症,約有4成至5成患者可維持腸道黏膜癒合。根據國外大型追蹤研究報告,使用生物製劑長期治療,約可降低3成潰瘍性大腸炎和7成克隆氏症需要手術切腸的風險。
由於類固醇、免疫調節藥物和生物製劑都可能增加感染的風險,因此使用前必須確認患者是否處於肺結核潛伏感染或是有B型肝炎、C型肝炎帶原的狀況,以避免治療過程中感染復發。
貼心小提醒
發炎性腸道疾病是自體免疫疾病,無法完全治癒,但目前已經有成效良好的藥物可以穩定控制發炎,改善預後。郭震亞醫師叮嚀,治療目標除了要改善腹痛、腹瀉、血便等症狀,更重要的是達到腸黏膜癒合,以降低出現嚴重併發症的機會,避免動刀切腸子!


