
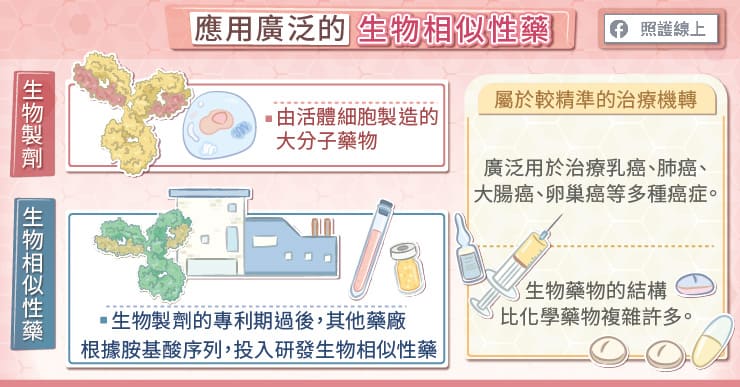
近年來生物製劑的發展相當迅速,使用範圍也愈來愈廣泛。義大醫院藥劑部項怡平部長指出,生物製劑是由活體細胞製作的藥物,是大分子藥物,能針對特定受體發揮作用,屬於較精準的治療機轉,可用來治療包括乳癌、大腸癌、肺癌、卵巢癌等多種癌症,也運用於多種自體免疫疾病。
所謂的「生物相似性藥」指的是與一個生物製劑相似的藥物,因為在生物製劑的專利期過後,其他藥廠可以根據該生物製劑的胺基酸序列來研發生物相似性藥。
由活體細胞製作的生物藥物,和由化學反應製作的藥物有極大不同,生物藥物的分子量大很多、結構也更為複雜。
要製作生物藥物,得先將一段特定的DNA序列利用載體植入活體細胞,經過培養後,活體細胞會根據DNA序列製作出胺基酸序列,並進一步組合成四級結構。
項怡平部長說明:「由於製程非常複雜,製作生物藥物的門檻很高,不是一般小規模藥廠有能力製作的。」
生物相似性藥也需要通過臨床試驗
生物製劑的機轉較為精準,能發揮一定的治療成效,但是因為研發難度高、製程又複雜,藥價往往比較高。而傳統化學藥物的結構相對較單純,在找出化學反應的步驟後,其他藥廠便能製作出完全相同的化學結構藥物,稱為學名藥。至於大分子的生物藥物,在製造過程中會受到很多因素的影響,即使胺基酸序列相同,成品也不盡相同,因此被稱為「生物相似性藥」。
生物相似性藥與生物製劑的研發重點不同,項怡平部長分析,「原廠對於生物製劑的製程有自己的獨家製程,屬於機密,所以其他藥廠必須從零開始,自行開發全新標準製程,才有辦法做出生物相似性藥。而這需要具備製作生物藥物經驗、較大規模的藥廠才有辦法進行。」

「分析參考藥物」為研發生物相似性藥的首要步驟,量化各種「關鍵品質屬性(critical quality attribute,CQA)」,包含主結構、立體結構、生物功能、安定性、受體結合與免疫化學特性等。
第二步-「打造全新標準製程」將DNA序列植入活體細胞,由活體細胞製作胺基酸序列並組合成四級結構,而研發期間需要反覆進行比較性測試。
第三步-「確立生物相似性」,分析各項數據,其相同性愈高,代表生物相似性藥與參考藥物間臨床差異愈小。
第四步-「進行臨床試驗」選擇高敏感度的受試者族群以及臨床指標,評估生物相似性藥是否與參考藥物之間存在顯著的臨床差異。生物相似性藥須完成臨床試驗,證明其療效、安全性皆和參考藥物相等,既非劣於、也不優於參考藥物,才能申請上市。
生物相似性藥增加治療可近性,讓更多患者受益
項怡平部長解釋,「對於一些需要自費使用的病患來說,生物相似性藥能夠減輕其經濟負擔。」近幾年來已有多種生物製劑被開發出來,專利也陸續到期,相關之生物相似性藥也都進入研發階段,部分生物製劑甚至有多家具規模的藥廠投入研發生物相似性藥。在愈來愈多樣的生物相似性藥被開發出來後,不僅能提供給患者更多選擇,也有助於降低政府的醫療負擔,讓有限資源可以得到更充分的利用。目前,世界各國對於生物相似性藥都有制定完善的法規,例如美國[1]、日本[2]、澳洲[3] 、歐盟[4]、台灣[5]、韓國[6]等,皆已核准通過多種生物相似性藥。

生物相似性藥的研發、核准過程皆相當嚴謹,上市之後政府會持續進行藥物監測與定期安全性報告,以確保生物相似性藥之品質、療效、安全性皆與參考藥物沒有臨床差異,保障生物相似性藥的品質與安全,以期讓患者安心使用。
1. U.S. Food and Drug Administration. Biosimilar Product Information. Retrieved from
https://bit.ly/2JBAKRK. Accessed in 12/2020
2. Division of Biological Chemistry and Biological, National Institute of Health Sciences, Japan Government. 日本で承認されたバイオ後続品. Retrieved from https://bit.ly/39Ry3WE. Accessed in 12/2020
3. Department of Health, Australian Government. (2020, December 03). Which biosimilar
medicines are available in Australia. Retrieved from https://bit.ly/3oxLvD9. Accessed in
12/2020
4. European Medicines Agency. Retrieved from https://bit.ly/39PgZR5. Accessed in 12/2020
5. National Health Insurance Administration, Ministry of Health and Welfare, Taiwan government.台灣生物相似藥品核准上市清單. Retrieved from https://bit.ly/2VNHfmK. Accessed in 12/2020
6. Ministry of Food and Drug Safety, Korea Government. Biosimilar. Retrieved from https://bit.ly/2JNPBZ4. Accessed in 12/2020


