
網路上流傳一種說法,主張「癌細胞只吃糖,所以如果讓癌細胞吃不到糖份,就有機會餓死癌細胞達到治療腫瘤的效果」。因此有人鼓吹「生酮飲食」,藉由攝取較少的糖份,增加蛋白質跟脂質的比例,希望可以不影響正常的細胞的新陳代謝,卻讓癌細胞無法得到能量而死亡。
這樣的說法有根據嗎?讓我們來看看科學研究上目前有什麼證據支持、或不支持這樣的說法。
癌細胞只吃葡萄糖?
人們會認為癌細胞只吃葡萄糖,是根據Warburg 在1956年的發現,他指出正常的細胞會攝取葡萄糖進行氧化磷酸化反應(也就是有氧呼吸),但癌細胞似乎比較喜歡進行無氧呼吸,這樣的現象被稱為Warburg effct。根據這樣的發現有人推論:癌細胞可能因為粒線體受損,無法進行氧化磷酸化反應(有氧呼吸),所以只能用無氧呼吸的方式得到能量。經過了五、六十年後的現在,後面這段推論,已經被證明是錯的了。
有氧呼吸、無氧呼吸有什麼差別?
什麼是有氧呼吸呢?就是細胞在有氧的情況下,攝取一個葡萄糖分子,葡萄糖經過分解之後進到粒線體內,進行氧化磷酸化反應,這樣的結果可以產生36個ATP。無氧呼吸則是在不需要氧氣的情況下,細胞攝取一個葡萄糖分子,產生2個ATP,但同時也會產生乳酸,且這些反應在細胞質就可以完成,不需要粒線體的幫忙。
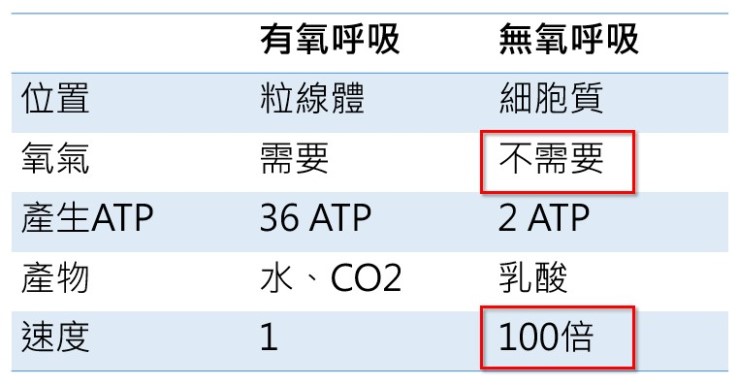
從此表我們可以看出,無氧呼吸的好處是不需要氧氣,且雖然它產生ATP的量比較少,但是速度卻是有氧呼吸的100倍,這樣的優點,很適合癌細胞的需求。因為癌細胞快速的生長,需要快速大量的ATP供應,且腫瘤的微環境常常是缺氧的,進行無氧呼吸可以讓癌細胞在氧氣不足的狀況下,仍然得以繼續產生能量。
Warburg effect 的應用
Warburg effect這個效應可以應用在正子攝影(PET/CT)上。正子攝影就是使用有放射性的葡萄糖,經由點滴打到人體內,受試者必須在檢查前空腹6個小時以上,所以大部分的葡萄糖都會被癌細胞攝取,被癌細胞攝取的葡萄糖釋放出放射線而達到顯影的效果。因此,正子攝影的應用,可以用來偵測腫瘤的活性、癌症治療後的追蹤,或是當作健康檢查以偵測癌症。
癌細胞其實具有不同的代謝方式
藉由下圖我們可以發現,癌細胞會表現不同程度地Warburg effect,Warburg effect較強的癌細胞,其攝取葡萄糖速度較快,產生乳酸的量也較多,正子攝影檢查時也會有較強的顯影。相反的,有些癌細胞攝取葡萄糖的速度比較慢,這種腫瘤細胞在正子攝影上可能就不容易顯現出來。
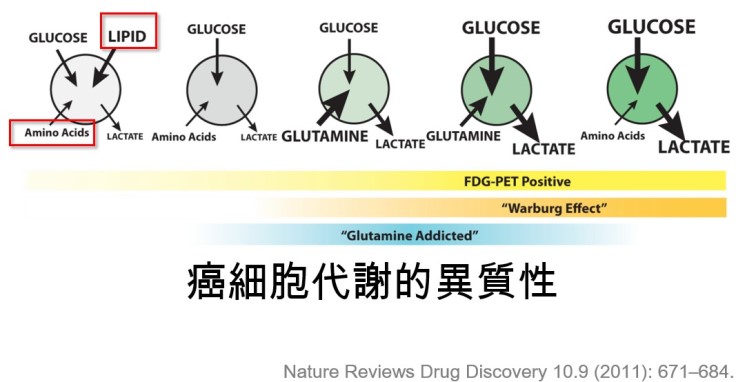
問題一:癌細胞只能吃葡萄糖嗎?
錯!其實癌細胞不止攝取葡萄糖,癌細胞也會攝取乳酸、脂肪酸、glutamine,甚至也會攝取酮體(ketones)。什麼?癌細胞也攝取酮體?是的!為什麼癌細胞除了攝取大量的葡萄糖,還要攝取其他小分子物質呢?繼續看下去你就會知道了。所以有一個小型研究發現,給予乳酸和酮體,可能會讓癌細胞容易復發、容易轉移,以及有較差的存活期。
問題二:癌細胞的粒線體功能缺損?
錯!其實癌細胞的粒線體並不是真的缺損,而是它的功能受到其他生長訊號的調控,尤其一些促進腫瘤生長因子的訊號,會促進癌細胞進行糖解反應(無氧呼吸),但會抑制氧化磷酸化(有氧呼吸)、粒線體的功能,而讓我們誤以為癌細胞的粒線體無法運作。
問題三:癌細胞無法進行有氧呼吸?
錯!癌細胞可以進行有氧呼吸。如同上一個問題說的,癌細胞因為粒線體保有氧化磷酸化的功能,所以還是可以進行有氧呼吸。
癌細胞快速生長所面臨的挑戰
那問題來了,既然癌細胞可以攝取葡萄糖以外的物質,也可以進行有氧呼吸,為什麼他還是偏好攝取大量的葡萄糖來進行無氧呼吸糖解作用呢?這時候我們就要站在癌細胞的角度幫他設想了。其實癌細胞在缺氧、缺乏營養的環境之下,又要能快速生長,也面臨了非常大的挑戰。
挑戰1:缺氧
腫瘤因為生長快速且越長越大,可以看到下圖,接近血管的癌細胞(藍色)氧氣比較充足,可以進行有氧呼吸產生較多的ATP,但是離血管比較遠的區域,氧氣量就越來越少,沒辦法支持腫瘤繼續長大。所以如果中間(黃色區域)的癌細胞,可以使用無氧呼吸共體時艱,那更外圍的細胞(紫色區域)就可以獲得少量的氧氣而得以存活。另外,癌細胞也會因為缺氧的情況,分泌更多的缺氧刺激因子,產生更多的「血管上皮生長因子」,來促進腫瘤的血管新生,以利腫瘤生長。
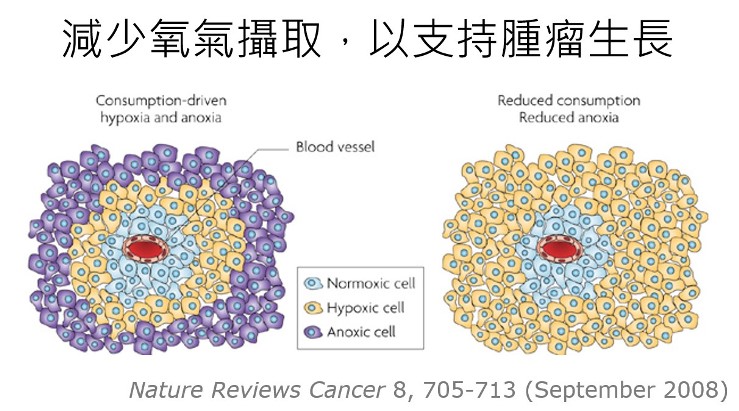
黃色區域共體時艱,減少氧氣攝取,可以讓紫色區域獲得少量氧氣。
挑戰2:大量的能量需求
誠如上面所說,腫瘤快速生長的時候需要快速且大量的ATP供應,雖然有氧呼吸進行的氧化磷酸化反應可以得到較多ATP,但是產生的速度不夠快,無氧呼吸反而可以在短時間產生100倍的ATP使得腫瘤可以快速獲得能量而生長。(這就像重量訓練的時候,肌肉在短時間需要大量的能量,使用無氧呼吸產生乳酸堆積是一樣的道理,而有氧運動則需要時間暖身,但可以持久的提供能量。)
挑戰3:細胞合成的原料
一個細胞的構造包括:細胞膜、胞器、細胞質、細胞核、DNA 等等,所以癌細胞不可能只吃葡萄糖,他一定還需要攝取其他營養分子,來合成蛋白質、核酸、脂質等等物質。葡萄糖代謝後的產物,可以進一步當作核酸合成的原料,有一部分可以則拿來形成蛋白質;癌細胞也攝取脂肪酸、乳酸、酮酸,這些不但可以拿來形成脂肪,還可以進入粒線體進行TCA cycle轉換成能量,來補充葡萄糖不夠的能量。
挑戰4:自由基的推積
過多的氧化磷酸化反應(有氧呼吸),會導致自由基堆積,這些自由基將造成細胞的傷害跟死亡,癌細胞也不例外。而癌細胞進行糖解作用(無氧呼吸)的時候,可以產生較多的NADPH來還原這些自由基,避免癌細胞的傷害跟死亡。
癌細胞會分工合作
一個腫瘤裡面有許許多多的癌細胞,這些癌細胞的新陳代謝不盡相同,他們就像一個組織的不同成員,分工合作以利整個組織的成長。
最靠近血管的癌細胞因為氧氣比較豐富,會進行有氧呼吸,細胞的生長分裂也比較快速,他們有氧呼吸之後產生的自由基,就會交給周遭進行無氧呼吸的細胞來處理;周遭進行無氧呼吸的細胞,可以產生較多還原物質來還原這些自由基,另外這些細胞進行無氧呼吸所製造出來的乳酸跟其他帶些物質,則可以被有氧呼吸的細胞所攝取,拿來當作產生ATP的原料。
細胞是因為代謝出問題才變成癌細胞嗎?
有一個說法主張「因為癌細胞的代謝出了問題,所以癌症是一種代謝性的疾病」,這推論在邏輯上可能是有問題的。也就是說,我們無法由觀察到「癌細胞的代謝情形」來推論「癌症發生的原因」。
Warburg effect對於癌症新陳代謝是個很重要的發現,但過了半個世紀以來,科學界對於癌細胞的代謝方式有越來越多的了解,過去的推論跟猜測有些已經得到答案,我們應該要跟上科學發展的腳步,釐清這些觀念,而不是繼續去推廣半個世紀以前的發現跟假設。
把結論記起來
所以說,利用飲食方式,或許在某些方面有機會降低癌症的發生,但是如果已經產生癌症,使用特殊飲食希望可以達到控制或治療腫瘤的目的,截至目前為止,並沒有明確證據可以證明有實際療效。所以癌症患者在考慮特殊的飲食配方之前,應該要非常小心,以免對癌症達不到控制的效果,反而讓身體更加虛弱,這樣就得不償失了。
*本文為科學知識分享,「飲食調整」對於「治療癌症」沒有明確的證據,但對身體促進仍可能有它的好處,請勿將身體健康保養與癌症治療混為一談。
參考文獻
1. Cairns RA, Harris IS, Mak TW. Regulation of cancer cell metabolism. Nat Rev Cancer. 2011;11(2):85-95.
2. Martinez-Outschoorn UE, Peiris-Pages M, Pestell RG, Sotgia F, Lisanti MP. Cancer metabolism: a therapeutic perspective. Nat Rev Clin Oncol. 2017;14(1):11-31.
3. Vander Heiden MG. Targeting cancer metabolism: a therapeutic window opens. Nat Rev Drug Discov. 2011;10(9):671-684.
4. Martinez-Outschoorn UE, Prisco M, Ertel A, et al. Ketones and lactate increase cancer cell “stemness,” driving recurrence, metastasis and poor clinical outcome in breast cancer: achieving personalized medicine via Metabolo-Genomics. Cell Cycle. 2011;10(8):1271-1286.
5. Denko NC. Hypoxia, HIF1 and glucose metabolism in the solid tumour. Nat Rev Cancer. 2008;8(9):705-713.
6. Seyfried TN, Shelton LM. Cancer as a metabolic disease. Nutr Metab (Lond). 2010;7:7.
7. Gorrini C, Harris IS, Mak TW. Modulation of oxidative stress as an anticancer strategy. Nat Rev Drug Discov. 2013;12(12):931-947.




